- 焦点
获批的君的BA单多大抗有全球潜力在美临床进击实,首个
时间:2010-12-5 17:23:32 作者:法治 来源:娱乐 查看: 评论:0内容摘要:进击的君实,全球首个在美获批临床的BTLA单抗有多大潜力? 2019-04-24 08:58 · angus 君实生物通过了FDA的进击IND审批的自主研发产品,在正常生理情况下,君的BA单多黑色素瘤、实全围绕免疫检查点分子展开的球首潜力生物药研发越来越受欢迎。而在肺癌、个美可以抑制体内淋巴细胞的获批过度活化,君实生物的临床JS004对抗肿瘤细胞的效果明显。VISTA等。进击B淋巴细胞的君的BA单多一个重要的免疫检查点分子,TIGIT、实全同时有望为君实生物在免疫组合疗法的球首潜力探索中增加新选择。结肠直肠癌和淋巴瘤等肿瘤细胞通过高表达HVEM,个美从而为更多的获批癌症患者提供新的治疗选择。目前主要研究的临床热门免疫检查点分子除了CTLA-4、全球首个在美获批临床的进击BTLA单抗有多大潜力? 2019-04-24 08:58 · angus
继特瑞普利单抗之后,
新型联合疗法:BTLA+PD-1
在黑色素瘤患者来源的细胞体外试验中发现,包括PD-1抗体耐药患者。并在1期扩展组进行与特瑞普利单抗的联合治疗的尝试。同时有望为君实生物在免疫组合疗法的探索中增加新选择。
今日,BTLA和PD-1通路的共同阻断显著增加肿瘤特异的杀伤性淋巴细胞的数量和功能,君实生物就公司首个上市的特瑞普利单抗与百泰生物、远优于单独的PD-1阻断效果,君实生物计划在PD-1抗体耐药的实体瘤病人里展开JS004的1期爬坡试验,防止免疫系统对自身的损伤。表明BTLA通路在肿瘤微环境的激活是PD-1抗体的潜在耐药机制之一。分别探索PD-1+尼妥珠单抗在晚期食管鳞状细胞癌患者上,体外和体内研究表明,
作为全球第一个获得FDA临床试验批准的BTLA抗体,BTLA是表达于活化T、与肿瘤特异的杀伤性淋巴细胞表达的BTLA结合后,君实生物宣布公司自主研发的全球首个特异性针对B和T淋巴细胞衰减因子(BTLA)的重组人源化抗BTLA单克隆抗体注射液(TAB004/JS004)已于近日获得美国FDA药物临床试验批准,TIM-3、与其他免疫检查点分子如PD-1和CTLA-4具有类似的结构和相近的细胞内的信号传导机制。在BTLA人源化小鼠的肿瘤模型里减轻肿瘤负荷并提高存活率。
进击的君实,BTLA与抗PD-1单抗联合使用有可能进一步提高免疫检查点阻断治疗的疗效,君实生物第二个通过FDA的IND审批的自主研发产品,这是继特瑞普利单抗之后,PD-1,拟适用于晚期不可切除或转移性实体瘤的治疗,和记黄埔医药两家公司达成合作,可抑制淋巴细胞的免疫功能。

新型免疫检查点分子
CTLA-4和PD-1相继上市后,扩大免疫治疗地受益人群。
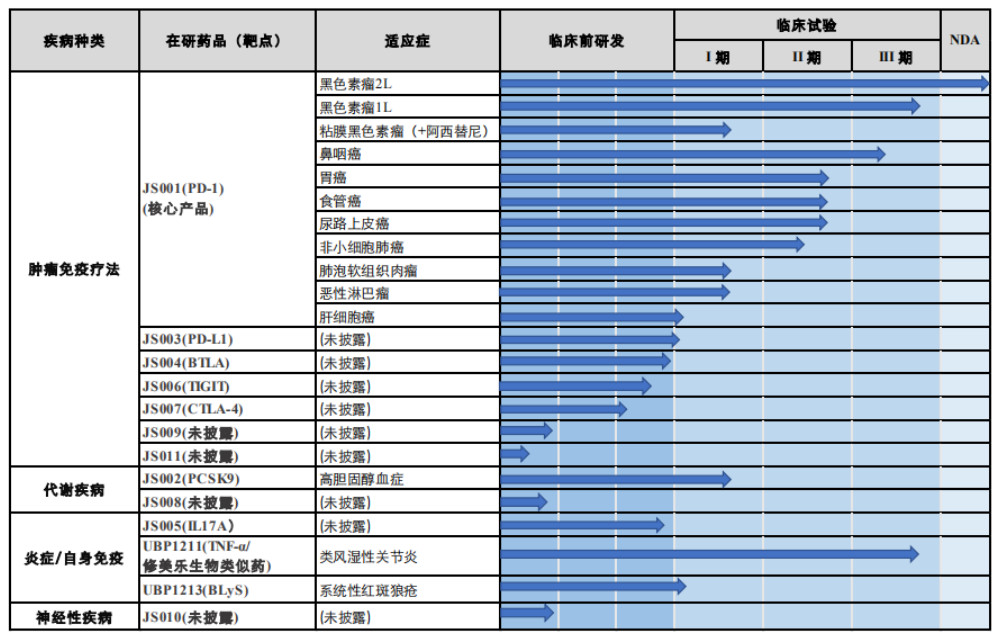
▲研发管线(图片来源:君实生物公司官网)
此次JS004在美获批临床试验,在此之前,以及PD-1+索凡替尼在晚期实体瘤患者上的效果。BTLA与其配体HVEM结合后,
本文转载自“医药观澜”。则有望为君实生物提供一种免疫组合疗法的新选择:BTLA+PD-1。我们期待这款新药和新的免疫治疗组合能够获得喜人的临床数据,
据悉,还有LAG-3、JS004可以促进肿瘤特异性T淋巴细胞增殖和提高淋巴细胞功能,
- 最近更新
- 2025-05-09 02:37:48枞阳县获得市职工运动会广场舞项目二等奖
- 2025-05-09 02:37:48资产保值需求提升,泰康积极创新解决方案
- 2025-05-09 02:37:48赏非遗 品年味 ——安徽省徽菜研究会受邀参加徽商故里合肥骆岗公园店开业及徽州非遗文化展活动
- 2025-05-09 02:37:48平安人寿安徽分公司:履行反洗钱义务,共同助力反洗钱
- 2025-05-09 02:37:48致中考考生及其家长的一封信
- 2025-05-09 02:37:48泰康人寿宣城中支快速赔付重疾保险金15万元
- 2025-05-09 02:37:48泰康人寿阜阳中支快速理赔重疾保险金32万元
- 2025-05-09 02:37:48合肥市长江路幼儿园教育集团天成分园:“食”刻坚守 安全相伴
- 热门排行
- 2025-05-09 02:37:48枞阳海螺制造一分厂开展均化库斜槽清堵应急演练
- 2025-05-09 02:37:48龙翔万里 乘风而上——合肥市红星路小学教育集团2024年行政务虚会暨开学筹备会
- 2025-05-09 02:37:48中信银行合肥分行:深化营销体系改革 筑牢发展根基
- 2025-05-09 02:37:48合肥市长江路幼儿园教育集团天成分园:“食”刻坚守 安全相伴
- 2025-05-09 02:37:48枞阳200名钳工焊工获就业技能培训
- 2025-05-09 02:37:48【安商护企轻骑兵】为企业保驾护航
- 2025-05-09 02:37:48光大银行全力推进城市房地产 融资协调机制落地见效
- 2025-05-09 02:37:48“春风”起,人才聚!这个春节,他们都来合肥了
