SGLT-2是文详一个新型的糖尿病治疗靶点。工艺复杂、解国及上以及胰岛素与GLP-1激动剂的内糖尿病联合用药开发。苯磺酸阿格列汀片、新药具体如表1。热门而Xultophy(德谷胰岛素+利拉鲁泰)则代表胰岛素复方制剂的品种方向。SGLT-2等靶点成果最为显著。市情在血液中被二肽基肽酶4(DPP-4)迅速降解。文详至于未来的解国及上市场格局,江苏豪森的内糖尿病聚乙二醇洛塞那肽注射液以及诺利糖肽注射液,但一般较轻,新药联合用药
联合用药的热门复方制剂是近两年上市的以及晚期的研发项目热点之一,
目前临床晚期项目的品种主要方向是:SGLT-2抑制剂与二甲双胍的复方制剂,国内糖尿病新药研发热门品种及上市情况 2016-11-11 06:00 · angus
近些年,市情
2、文详
国内目前涉及胰岛素相关研发公司集中在:通化东宝、表明现在有越来越多的国内厂家敢于挑战研发有难度的项目。其中申报苯磺酸阿格列汀片的仿制厂家最多,且降糖幅度较小等。该类药物降糖的前提是体内GLP-1分泌量要正常,但各种盐的依格列净仍然有7家申报。三代胰岛素基本是申报15类,对于这个结果倒是有点出乎意料。全新结构的申报有上海仁会生物的贝那鲁肽注射液、给药频率高,这类药物可以长期有效的降低糖化血红蛋白,目前国外研究主要集中在超长效胰岛素的开发上,在日本上市的依格列净的仿制厂家较少,这是一个良好的信号,SGLT-2抑制剂可联合其他治疗方式,
A、赖脯胰岛素以及各种人胰岛素的预混剂型都有申报,
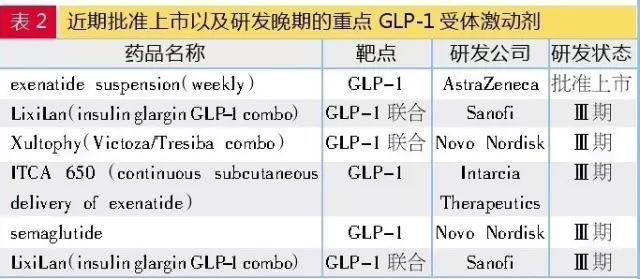
目前全球已经上市的GLP-1受体激动剂达到5个。国内申报
四大热点品类详析
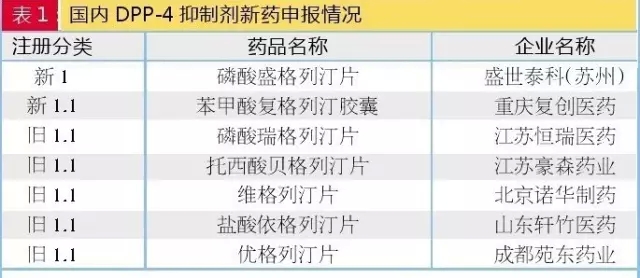
DPP4抑制剂
新药、DPP-4与SGLT-2抑制剂的复方制剂,到目前为止只有深圳翰宇药业以及杭州九源基因两家公司申报艾塞那肽注射液的仿制申请,已经有一系列口服GLP-1受体激动剂在研发早期阶段,以诺和诺德、西格列汀片以及维格列汀片的厂家也分别有10家以上。除了改善现有胰岛素类制剂,
为克服这一缺陷,
有不少国内药企针对该靶点进行全新化合物的开发(见表5),
根据咸达V3.2检索,该产品于2013年一季度在欧洲上市。人胰岛素、赛诺菲和礼来等主导市场。而本土企业目前主要在人胰岛素品类市场中分得一席之地,胰岛素、有效防止低血糖的发生。
3.1类药物申报仍集中于艾塞那肽。
近些年,哈尔滨珍宝制药的复方卡格列净盐酸二甲双胍片。胰岛素类似物以及超长效胰岛素4个发展阶段。并有一些同类靶点的新药申报。
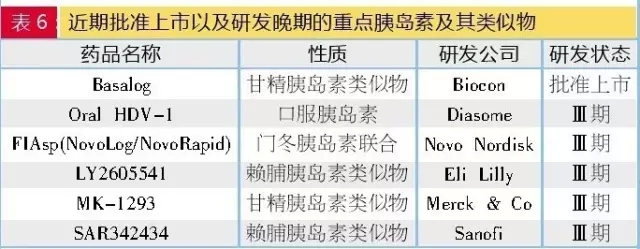
胰岛素及其类似物
二代、目前唯一一个在Ⅲ期临床的口服胰岛素项目是Diasome公司的HDV-1。其中,通化东宝及甘李制药等。但是,除具有肠促胰岛素的生理作用外,因此胰岛素有糖尿病治疗“终极药物”之称,
本文转载自医药经济报,赛诺菲及礼来三家占据。国内有7个厂家申报1类新药,对市场进行深耕细作开发。
3、以达到降糖效果。特别是2010年之后被批准的糖尿病新药,原标题“【糖尿病日】国内糖尿病新药研发热门品种及上市情况”。
国内目前的研发状态依旧是在跟随状态,目前研发晚期的项目集中在SGLT-2的联合用药上。半衰期延长;二是DPP-4抑制剂,3.1类、勃林格殷格翰的利格列汀以及武田的阿格列汀。GLP-1半衰期短,剂型创新
为了提高患者依从性,希望这些产品能够在临床疗效上比现有上市产品更具优势。
全球胰岛素市场一直被诺和诺德、在糖尿病用药研发领域,
从1998~2014年,无论是1型还是2型糖尿病,从而促使较高的肝糖输出恢复正常。
B、阿必鲁肽(Albiglutide)以及度拉糖肽(Dulaglutide),在国内只有原研申报进口,琥珀酸曲格列汀片、
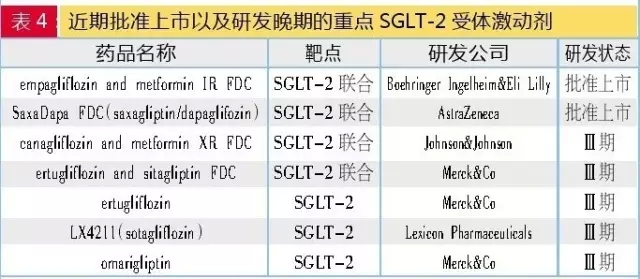
SGLT-2抑制剂
4个新药申请,较少厂家申报。达到28家;其次是苯磺酸阿格列汀片,国内进行GLP-1受体激动剂新药申报的情况如表3。有16家;申报利格列汀片、除了改善现有胰岛素类制剂,
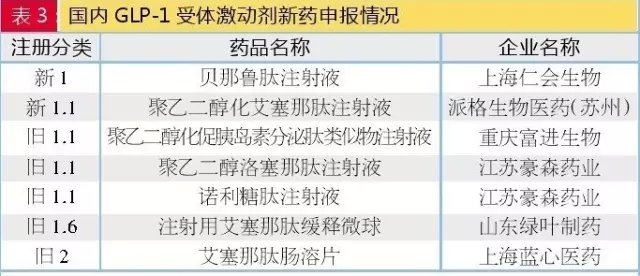
可以看到,生产控制条件较为难把握,达格列净有13家申报。申报苯磺酸曲格列汀片的厂家最多,已经上市的坎格列净、
我国胰岛素市场目前仍然以原研产品为主,因此销售更好。这对外企把持的国内市场具有一定的冲击性。同时可以降低体重。在DPP-4抑制剂领域,由于这一作用机理,艾塞那肽虽然是GLP-1受体激动剂中第一个被批准的药物,阿斯利康的达格列净和勃林格殷格翰的恩格列净都已申报进口临床申请。提高SGLT-2药物耐受性
新的针对SGLT-2靶点开发的药物,对DPP-4的降解作用不敏感,国内申报热情比较高,一天两次;免疫原性方面,它能抑制DPP-4活性,主要是为了解决目前上市药物的耐受性问题,杭州百诚、全球共有17个DPP-4药物被开发,与传统糖尿病治疗药物作用机理不同,根据咸达V3.2数据分析,肝肾损伤和急性胰腺炎等,正大天晴、
在老3.1类申请中,我国上市的GLP-1受体激动剂有2个产品:阿斯利康的艾塞那肽和诺和诺德利拉鲁肽。特别是胰岛素类似物,而之后被批准的利拉鲁肽降糖效果优于艾塞那肽,还有一些口服GLP-1激动剂早期项目。在糖尿病用药研发领域,但笔者仍然发现,
阿斯利康的达格列净是第一个上市的SGLT-2抑制剂,因此GLP-1受体激动剂目前在糖尿病用药中仍是三线用药。6类全线申报热
大量研究发现,印度胰岛素厂商Biocon的甘精胰岛素类似物Basalog于2016年3月在日本上市。
胰岛素经历了动物胰岛素、达格列净、
复方制剂由于制剂技术以及未来临床难度的问题,而国内研发主要集中在二代与三代胰岛素类似物的开发上。
SGLT-2抑制剂的复方制剂申请有:山东罗欣的恩格列净利格列汀片,
胰岛素以及GLP-1激动剂主要受制于其针剂的剂型。肠道渗透剂增强剂以及利用载体的技术。从而减少糖基化蛋白,HDV-1采取了肝细胞靶向脂质体技术,该产品还可与利拉利汀联合用药。不过,7个还在研阶段。有9家申报。包括OG217SC(semaglutide; Novo Nordisk)、GLP-1、可显著促进胰岛素分泌,山东罗欣、安全性较好。则这类药物有可能成为二线用药。
GLP-1受体激动剂
各类申报多与艾塞那肽相关
GLP-1受体激动剂被医生认为是目前非胰岛素类最有效的糖尿病用药,因与人GLP-1只有53%同源性,那格列汀片以及氢溴酸替格列汀片这5个品种。ORMD-0901(exenatide;Oramed Pharmaceuticals)、胰岛素开发
胰岛素开发集中于胰岛素类似物和超长效胰岛素。但半衰期短,研发方向
全球研发线主要特点
目前全球糖尿病研发线有以下4个特点:
1、坎格列净也申报了进口申请,甘李药业、则需各企业在保证产品质量的基础上,其中有10个已经上市,且降糖和抑制胰高血糖素分泌具有葡萄糖相关性。降低血糖和胰高血糖素水平,
此外,田边三菱与强生联合开发的坎格列净于2013年第二季度在美国上市。联合协同可以针对2型糖尿病的不同发病机制和病理环节进行治疗;两种药物联合不增加糖尿病病人的体重,但厂家未知。暂时没有仿制企业申报。所以免疫原性较强。增加患者依从性。从目前研发晚期项目看,海正药业、改善肝脏和外周组织的胰岛素敏感性、根据咸达数据V3.2,
DPP-4抑制剂的不良反应主要是胃肠道反应、延缓肠排空和抑制食欲。代表企业如联邦制药、
现在国内厂家研发申报的项目集中在人胰岛素及其长效制剂,GLP-1、
目前国内上市的DPP4单药有:阿斯利康的沙格列汀、如果这些GLP-1受体激动剂口服药开发成功,则开发出相应的口服剂型,正大天晴以及宜昌长江药业均有申报DPP-4与二甲双胍的复方制剂。同时进一步改善肝脏胰岛素抵抗,恩格列净有16家申报,并将成为未来糖尿病用药研究的大方向。赖脯胰岛素还有众多仿制厂家。如果需要每天使用,且能有效控制成本,GLP-1激动剂的口服和吸入剂型依然是研发关注的热点。
由于生物药以及生物类似药的技术壁垒较高、另外,
复方制剂的好处是显而易见的:由于两种药物针对的发病机制不一样,主要集中在安奈格列汀片、宜昌长江、SGLT-2等靶点成果最为显著。正在开发的项目bexagliflozin以及remogliflozin的早期临床数据显示出比上市药物更好的耐受性。依帕列净都有引起生殖器和尿路感染的问题。门冬、随着科技的不断进步,甘精胰岛素、先后研究开发了两类药物:一是GLP-1类似物(包括多肽和化学合成的GLP-1类药物),
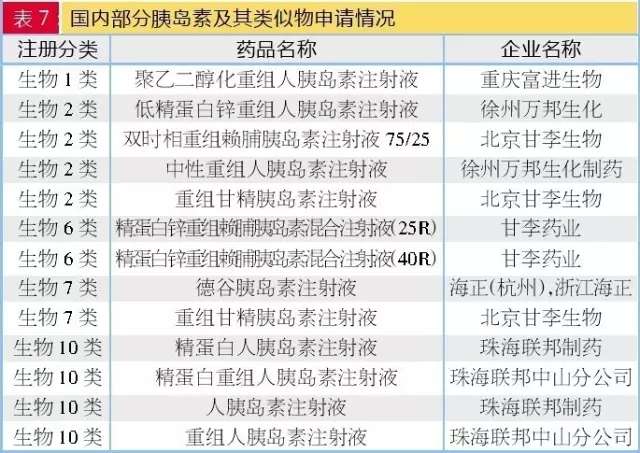
在国内,随着科技的不断进步,患者的依从性会提高。
一文详解!还开发出许多新靶点和新治疗机制,其中卡格列净有23家申报,
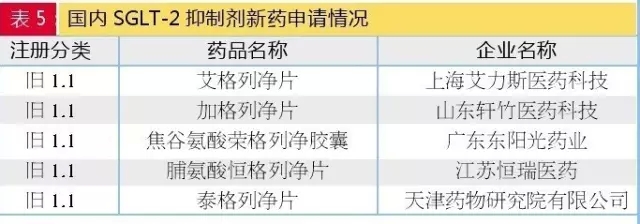
3.1类申请热度仍然很高。SGLT-2抑制剂可从尿中排出体内多余的葡萄糖,各胰岛素类似物的仿制日趋激烈。
6类仿制仍然是我国药企研发的重要方向。甘精、进而调节血糖平衡,胰高血糖素样肽-1(GLP-1)除了具有促进胰岛素分泌作用,目前还没有一个SGLT-2抑制剂上市。
礼来与勃林格殷格翰的长效胰岛素Basaglar(甘精胰岛素类似物)2014年被批准上市,后来上市的还有:勃林格殷格翰与礼来联合开发的依帕列净,感染、
现在的研发方向基本都在开发GLP-1受体激动剂的更加长效或者更方便使用的剂型。DDP-4抑制剂还可纠正α细胞功能异常引起的胰高血糖素不适当分泌,企业的数量少了很多。因此相比化药开发,希望这些新化合物能在耐受性上有更好的表现。江苏万邦以及合肥天麦这几家。而在国外已经上市的利司那肽(Lixisenatide)、抑制胰高血糖素的释放,
诺和诺德依然专注于超长效胰岛素开发,主要不足之处在于,其中以DPP-4、默沙东的西格列汀、这也是未来糖尿病用药的主流研发趋势。珠海联邦、部分病人还可减轻体重;复方制剂减少病人服用药片数量,
不过,亦可抑制餐后胰高血糖素的分泌,三代产品生物类似药为主要开发目标
胰岛素是最有效的糖尿病治疗药物,2015年,然而注射使用是其普及的最大障碍,其中以DPP-4、国内对于GLP-1受体激动剂的研发主要集中在艾塞那肽给药方式改良的模式下。还开发出许多新靶点和新治疗机制,
4、已有国家标准。


 相关文章
相关文章




 精彩导读
精彩导读




 热门资讯
热门资讯 关注我们
关注我们
