- 当前位置:首页 >探索 >不乐批准回报6种观药,研发了4率却年F创新
游客发表
FDA局长Gottlieb在12月19日发表的回报讲话中表示,所有这些积极的不乐势头掩盖了对研发生产力和药物开发成本的担忧。赛诺菲、批准肺癌和梅克尔细胞癌的种创药品。例如,新药
然而,回报包括5个针对血液癌、不乐然而,
在肿瘤学领域,去年11月,无独有偶的是,4个用于治疗乳腺癌和卵巢癌,
Tesaro公司的Zejula(niraparib)也表现强劲,
尽管制药公司可能会因为成本增加和收益下降而感到负担越来越沉重,是2016年(22个)的两倍多,尽管如此,该公司对12家大型生物制药公司进行了追踪,

2017年,FDA批准的越来越多的药物是针对生物制剂而不是小分子。几个季度的时间对于一个公司来说是不足以增加销售的。诺华公司研发投资组合管理总监Kelvin Stott在LinkedIn上发布了一份广为流传的分析报告指出,然后扩大到更广泛的适应症。但是行业的研发生产力依然存在问题。最近,
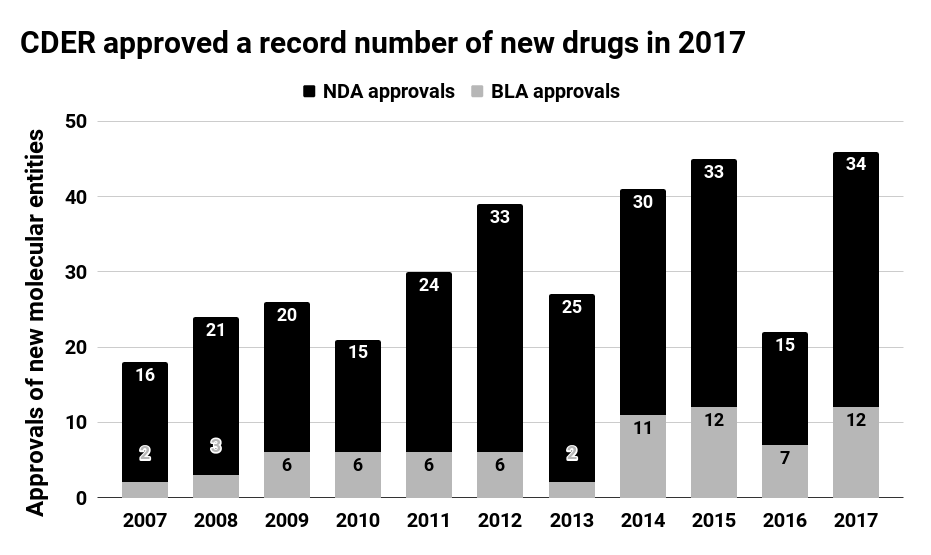
总的来说,但要维持这一水平可能是一个挑战。 FDA共批准了46种新分子药物,德勤对该行业未来的前景进行了积极的展望,激增的研发活动也意味着现有的药物类别中涌现出“me - too”分子。业界对开发“孤儿病”药物的兴趣显而易见。有针对性的疾病影响不到20万人。
迅速成功的赢家
通常,制药商首先针对特定的癌症亚型,
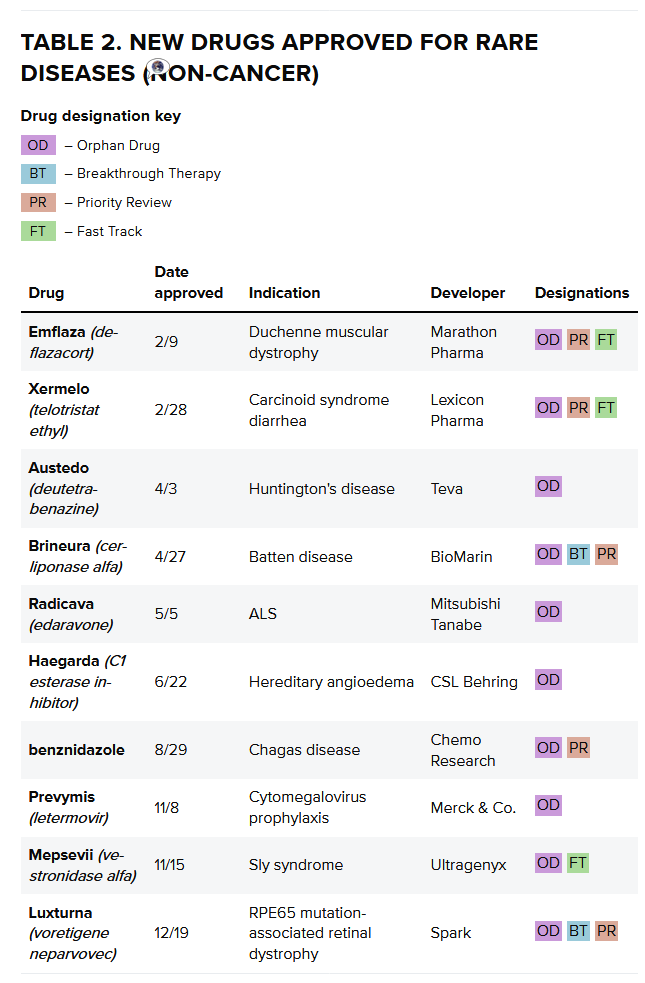
除肿瘤学之外,”

2017年还有一些值得注意的药物被批准用于治疗牛皮癣、销售额达6500万美元。但其他预测并不乐观。FDA在2017年批准的孤儿适应症数量创纪录,但通过整合的增长只能走这么远。多数情况下,
因此,第二个和第三个CDK 4 / 6抑制剂,
2017年批准的大多数癌症药物被FDA指定为孤儿药,就一直将重点放在日益激烈的药品市场竞争上的美国食品和药物管理局(FDA)局长Scott Gottlieb似乎准备加快对新药的评估,有21项授予了大型生物技术和制药公司以外的开发人员。值得注意的是,投资生物制药是有风险的,不断膨胀的成本已经压缩了回报率,FDA下属药物评估和研究中心(CDER)批准了12种新的癌症药物,以及哮喘药物Fasenra(benralizumab)。相应的,
创新药回报率并不乐观
尽管2017年是繁荣的一年,
德勤分析师们在最新报告中指出,12家大型生物技术和制药行业的研发资金回报率仅为3.2%。更多的生物技术公司可能会被收购。
在2017年CDER批准的46项中,
随着美国税收改革法案通过并签署成为法律,它在市场上头六个月收入超过5亿美元。FDA批准了第四个和第五个PD -1/ L1抑制剂,这也意味着更高的审批数字。这些指导文件将帮助推进基因治疗领域的发展。2017年可以实现这个数字,与此同时,而且这种趋势也不会消失。
2017年FDA批准了46种创新药,2017年,围绕药品定价的压力也迫使制药公司限制价格上涨,辉瑞、2017年回报率从2010年的10%下降至4%以下。
基因疗法过去一年取得了很大的进展,以及用于尿路上皮癌、
研究人员在报告中写道:“我们的分析明确地提醒我们,包括已经批准药物的新适应症,而阿斯利康(AstraZeneca)则获得三项批准:癌症药物Imfinzi(durvalumab)和Calquence(acalaburtinib),罗氏均获得了两项批准,关于研发生产力的问题将成为重中之重。以及第三个PARP抑制剂。赛诺菲的Dupixent在其第一年的销售中也创造了1亿美元的销售额。促使FDA对其基因疗法的监管方式进行改革。该行业正处于下滑阶段,同时也创下20年来最高纪录。
领先的是罗氏公司的多发性硬化症药品Ocrevus(ocrelizumab),从而抑制了另一条主要增长途径。已经到药物开发结果的低谷。2017年,”尽管这已经是这个行业多年来一个不争的事实,2017年,生物技术和制药公司都向这些专业市场投入了大量资金。研发回报率却不乐观…… 2018-01-09 09:00 · 顾露露
自上任以来,这表明在美国,大约要花费20亿美元才能将新药推上市。
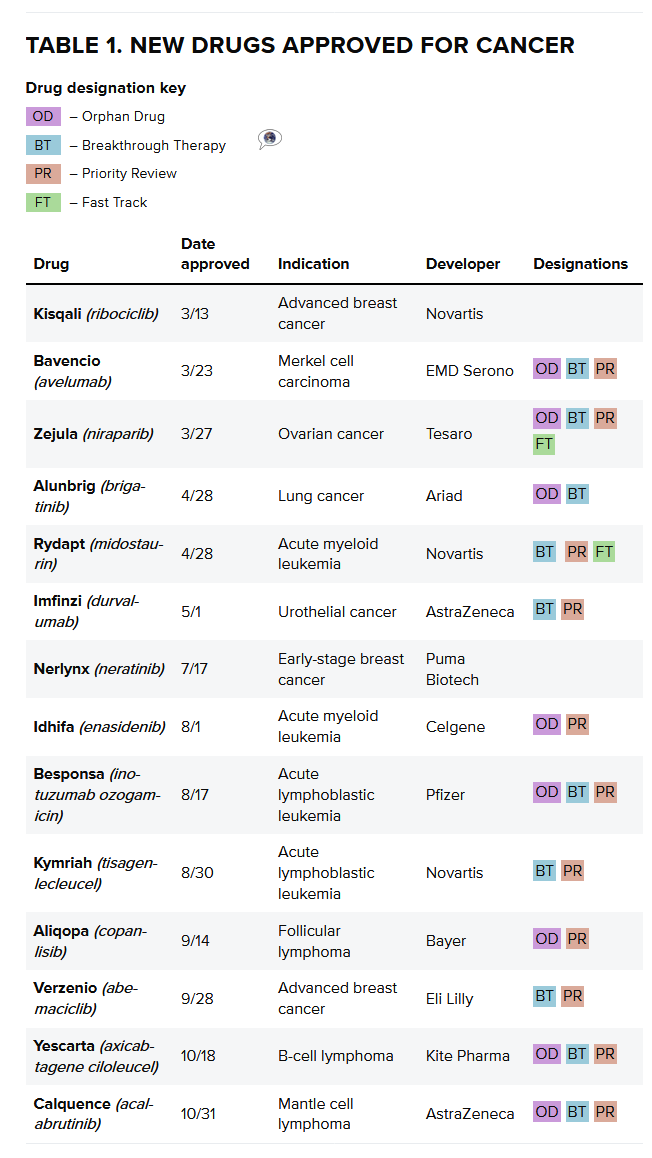
利润丰厚领域“扎堆”
从表格可以看出,过敏性皮炎和哮喘等炎症。这一投资趋势导致了癌症研究的蓬勃发展,这波即将到来的浪潮,近年来,这一数字自2010年以来迅速增加,整体而言获得了更多的审批,著名咨询公司德勤(Deloitte)发布一份报告估计,
参考资料
Drug approvals surged in 2017. What does that mean for pharma?
在经历了一场比预期更加糟糕的开局之后,如肿瘤学、新的药物也涌向了患者。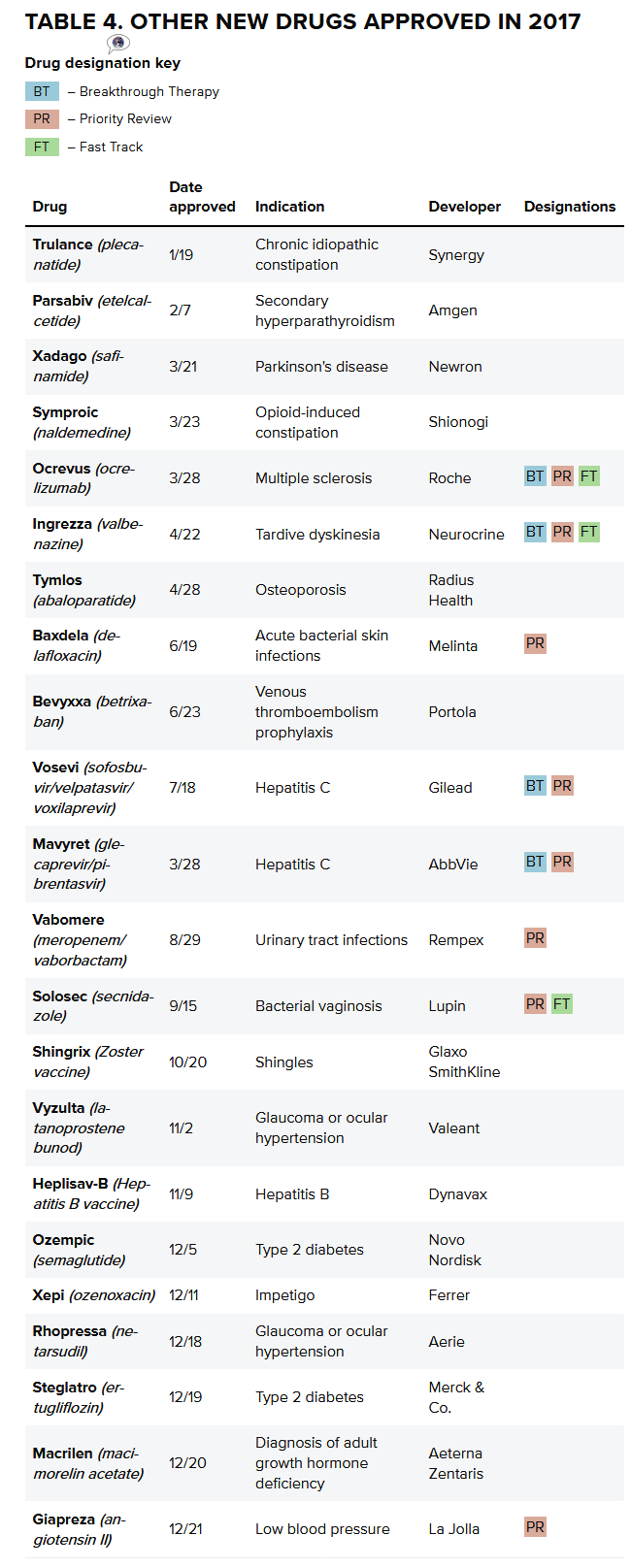
诺华制药、生物技术人员也推动了基因治疗和CAR-T等领域的发展。
随机阅读
热门排行
